Aplicaciones De La Ley De Avogadro
VOLVER AL ENUNCIADO DE ÉSTE Y DE OTROS EJERCICIOS RELACIONADOS CON LA LEY DE AVOGADRO. En 1811 enunció el conocido principio o ley de Avogadro basado en la teoría atómica de John Dalton y la ley de Gay-Lussac sobre los vectores de movimiento en la.

Quimica Ley De Gay Lussac Relacion Entre La Temperatura Y La Presion Youtube
La Ley de Avogadro es la cuarta de las leyes de los gases de la que nos ocupamosEsta ley relaciona el volumen y la cantidad numero de moles de gas a presión y temperaturas constantes.

Aplicaciones de la ley de avogadro. Debido a que en el ejercicio anterior se mantienen constantes la presión y la temperatura y se relacionan el volumen con el numero de moles se puede emplear la ley de avogadro para solucionar este ejercicio. About Press Copyright Contact us Creators Advertise Developers Terms Privacy Policy Safety How YouTube works Test new features Press Copyright Contact us Creators. M a O 16 uma.
Ya que la ley de avogadro sugiere una relación entre los volúmenes cantidades de gas a presión y temperaturas constantes se tiene que una de sus posibles aplicaciones a la vida cotidiana entraría en el llenado de un globo infantil al suministrar gas dentro del material este se expande lo cual a su vez permite el aumento de volumen de igual forma al dejar escapar un poco. La constante de Avogadro o número de Avogadro es el número de partículas constituyentes que se encuentran en la cantidad de sustancia de un mol. El principio de Avogadro.
Ley de Charles V1 T1 V2 T2- La puedes observar en un globo aerostático. Comportamiento de un gas a presión y temperatura constantesObjetivos- Comprender el comportamiento de un gas a presión y temperatura constanteEsta video c. La ley de Avogadro es de suma importancia en el desarrollo de la química ya que permite calcular el peso de los cuerpos que pueden cambiar de estado convirtiéndose en gases o vapor.
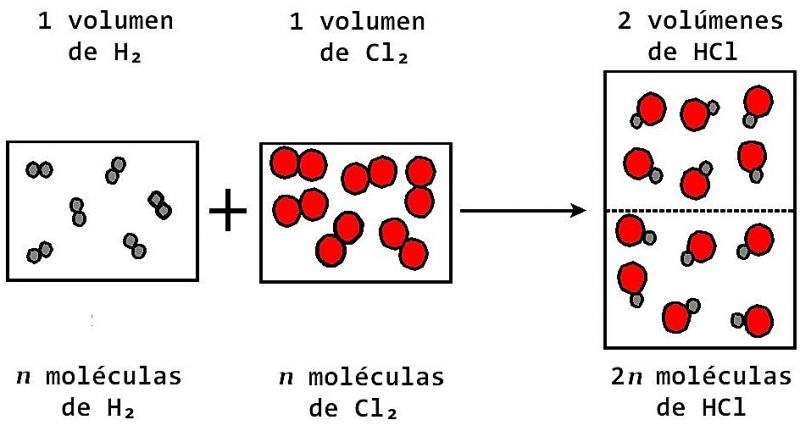
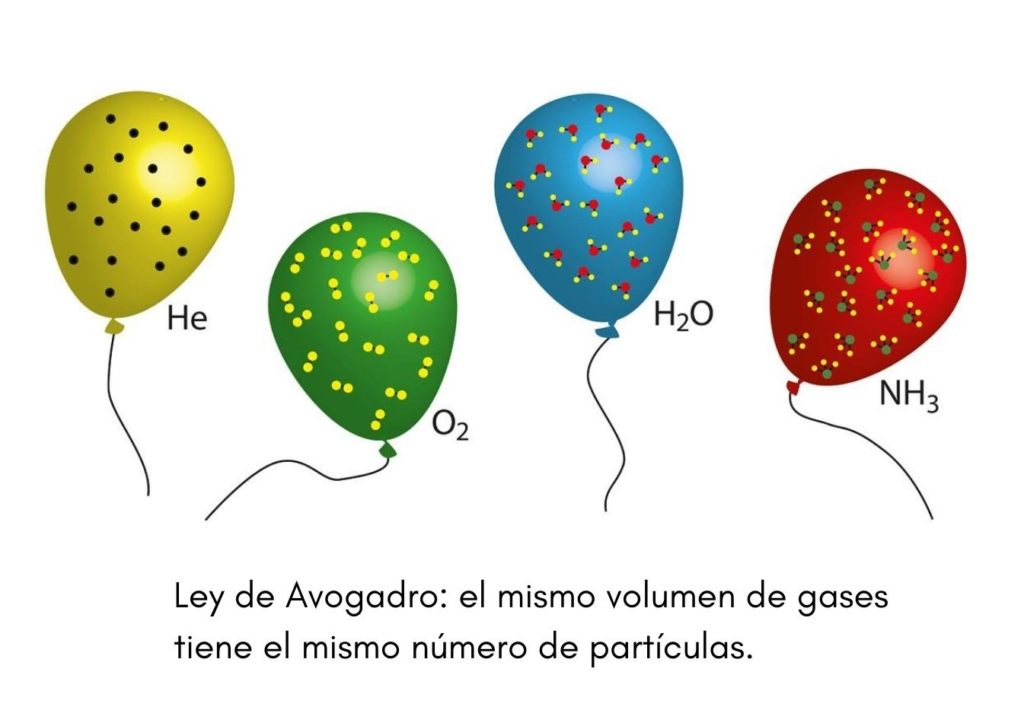
A presión y temperatura constantes la misma cantidad de gas tiene el mismo volumen independientemente del elemento químico que lo forme. Los resultados de ciertos experimentos con gases lo llevaron a formular una conocida Ley de Avogadro. Por partículas debemos entender aquí moléculas ya sean éstas poliatómicas o monoatómicas.
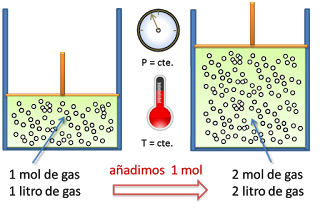
Ley de Avogadro. Principios de los gases Ley de Avogadro Descubierta por Avogadro a principios del siglo XIX esta ley establece la relación entre la cantidad de gas y su volumen cuando se mantienen constantes la temperatura y la presión. La Ley de Avogadro es una de las leyes de los gases ideales.
Toma el nombre de Amedeo Avogadro quien en 1811 afirmó que. A principios del siglo XIX un científico italiano Lorenzo Romano Amedeo Carlo Avogadro estudió la relación entre el volumen y la cantidad de sustancia del gas presente. Lo puedes observar en un globo que inflas a mayor presión ejercida el volumen del globo aumenta.
En 1811 Avogadro realiza los siguientes descubrimientos. Y sugirió la hipótesis. La ley de Avogadro a veces llamada hipótesis de Avogadro o principio de Avogadro o también hipótesis de Avogadro-Ampère es una de las leyes de los gases idealesToma el nombre de Amedeo Avogadro quien en 1811 afirmó con referencia a la ley de Gay-Lussac o ley de volúmenes de combinación.
N1 0025 moles 2 l 05 l 01 moles. M a H 1 uma. Asegura que en un proceso a presión y temperaturaconstante isobaro e isotermo el volumen de cualquier gas es proporcional al número demoles presente de tal modo queLey de.
La Ley de Avogadro es una de las leyes del gas. Ley de AvogadroLa Ley de Avogadro fue expuesta por Amedeo Avogadro en 1811 y complementaba a lasde Boyle Charles y Gay-Lussac. Por tanto es el factor proporcional que relaciona la masa molar de una sustancia la masa de una muestra.
INTERESA RECORDAR LA LEY DE AVOGADRO. Aplicacion de las leyes en la vida cotidiana Ley de Boyle P1V1 P2V2. B- Hallar la cantidad de átomos de hidrógeno en esa misma cantidad 35 mL c- Hallar la cantidad de átomos de oxígeno en esa cantidad 35 mL DATOS.
El trabajo del científico italiano Amadeo Avogadro complementó los estudios de Boyle Charles y Gay-LussacEnunciando la ley que lleva su nombre. Respuesta 01 moles de helio habian. Es sobre la base de la ley de Avogadro que la teoría atómico-molecular a partir de la teoría cinética de los gases comenzó su desarrollo.
Explicación de la ley de Avogadro. V1n1 V2n2 n1V1 n2V2 n1 n2 V1V2. Principios de los gases y aplicaciones.
La Ley de Avogadro es una ley de los gases que relaciona el volumen y la cantidad de gas a presión y temperaturas constantes. Ley de AvogadroArtículo principal.

Quimicas Ley De Avogadro De Los Gases
Ley De Charles Gases Fases De La Materia
Ley De Avogadro Que Es En Que Consiste Enunciado Formula Aplicaciones

Pdf Quimica Formularios Estequiometria Ley De Avogadro Yacatzint Mendoza Academia Edu
Http Catalinaartunduagasar Blogspot Com 2016 03 Gases En La Cotidianidad Html

Here S How To Use The Boyle S Law Formula For Ideal Gases Boyle S Law Charles Law Ideal Gas Law
Aplicaciones De La Vida Diaria Ley De Los Gases By Santiago Turriago Garcia

Aplicaciones De La Ley De Charles En La Vida Diaria Nueva Aplicacion

Ley De Avogadro De Los Gases Quimica Wikisabio

Ley De Avogadro Wikipedia La Enciclopedia Libre
Ley De Avogadro Que Es Formula Condiciones Importancia Ejemplos

Quimicas Ley De Avogadro De Los Gases

Ley De Avogadro Ejemplos Cotidianos









Post a Comment for "Aplicaciones De La Ley De Avogadro"