Ley De Henry Ejemplos
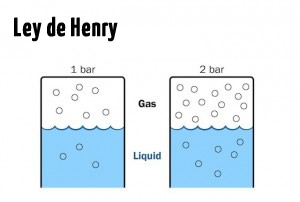
LEY DE HENRY La lata de refresco hace uso de laLey de Henry la cual dice que la cantidad de gas disuelta en un líquido es directamente proporcional a la presión que ejerce ese gas sobre el líquido. 3125 103 2 040 2 0625 2.
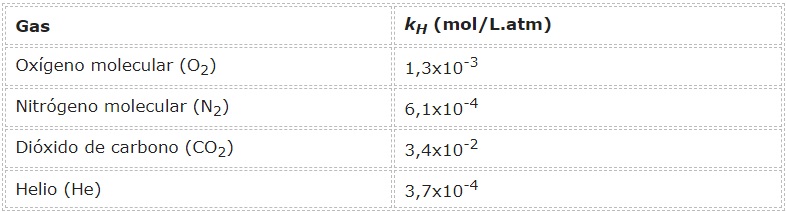
Ley De Henry Explicacion Formula Ejemplos Excepciones
Por ejemplo para la disolución de oxígeno en agua a 20 ºC la constante de Henry es 13610-5 mol L-1 kPa-1 eso nos permite calcular la solubilidad de.
Ley de henry ejemplos. La cantidad de gas disuelta en un líquido a temperatura constante es proporcional a la presión parcial del gas sobre el líquido. La ley de Henry se puede usar para determinar la presión parcial de un gas en el seno de un fluido. Video de apoyo para la Unidad de Aprendizaje Operaciones Unitarias I de la Licenciatura en Biotecnología de la UNADM.
El factor de proporcionalidad se llama constante de la ley de Henry. En química física la ley de Henry es una ley de los gases que establece que la cantidad de gas disuelto en un líquido es proporcional a su presión parcial sobre el líquido. Para el caso de los valores de la constate de la Ley de Henry presentados en esta base de datos la temperatura está expresada en grados Celsius.
S es solubilidad o fracción molar de equilibrio del gas en solución. Ley de Henry-Presión de vapor de las disoluciones - Disoluciones. Ejemplo A 0ºC y una presión de O2 de 100 atm la solubilidad del en agua es.
Entre ms se agrega ms disminuye la presin de vapor. Leyes de los gases y ejemplos 1. Textrm presion parcial frac textrm concentracion del gas disuelto textrm constante de HenryPz P x Xz Por ejemplo a 50 metros de profundidad 165 pies la presión absoluta es de 6 bar 1 bar correspondiente a la presión atmosférica 5 bar por la debida al agua y la presión.
Henry descubrió en 1803. Calculo de la constante ley de Henry. Establece que la solubilidad de un gas en un líquido es proporcional a su presión parcial y a su coeficiente de solubilidad a una temperatura constante.
Aplicamos la ley de Henry. La constante de proporcionalidad en la ley de Henry debe tener esto en cuenta. Como la soda usa dióxido de carbono cuando se abre la lata.
Leyes de los gases Por. La lata de refresco hace uso de laLey de Henry la cual dice que la cantidad de gas disuelta en un líquido es directamente proporcional a la presión que ejerce ese gas sobre el líquido. Con la Ley de Henry cerramos la parte de física aplicada al buceoRecordad que previamente hemos explicado al Ley de Boyle la Ley de Charles y la Ley de Dalton.
Qué es la Ley de Henry. Video de apoyo Unidad 3. - Solubilidad de gases.
La constante de proporcionalidad en la ley de Henry debe tomar esto en consideración. Como la soda usa dióxido de carbono cuando se abre la lata escapa el gas y el carbono disuelto se eleva hasta arriba y escapa de ahí el.
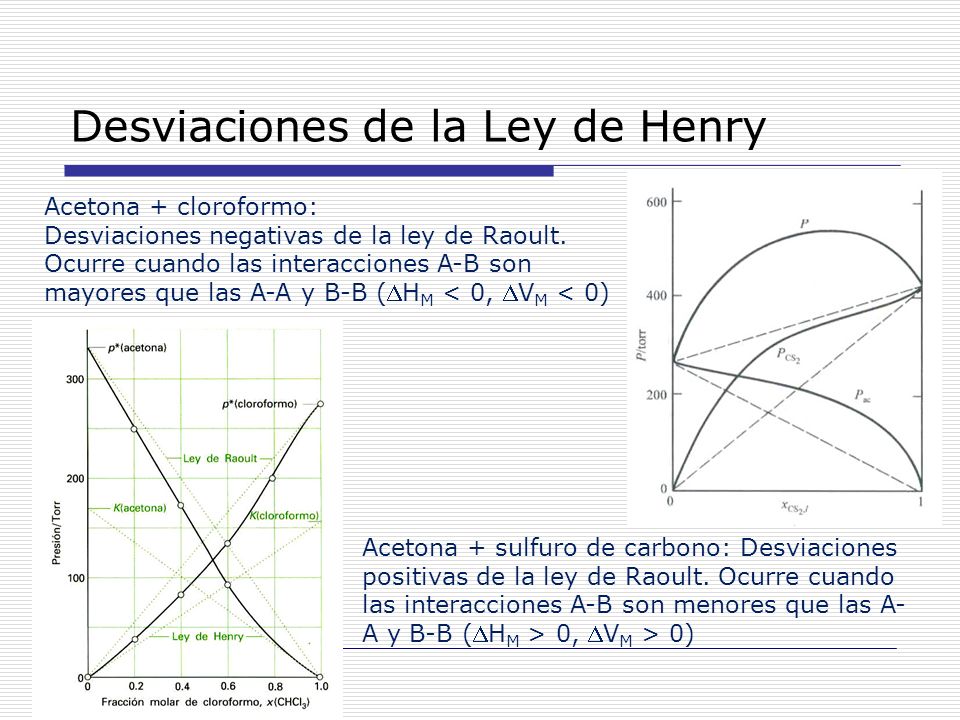
Las unidades de la constante que dependen de las unidades elegidas para expresar la concentración y la presión. Ley de Raoult Raoult encontr que cuando se agregaba soluto a un disolvente puro disminua la presin de vapor del disolvente. La ley de Henry es una ley de los gases formulada por el químico británico William Henry en 1803.
Esa ley dice que la solubilidad de un gas en agua depende de la presión parcial en esa ley varia con el gas y la temperatura y revive el nombre de constante de Henry. Por ejemplo en los procesos de intercambio de gases en la respiración cuando están en contacto con el plasma del cuerpo humano la solubilidad del dióxido de carbono es aproximadamente 22 veces mayor que la del oxígeno. Por esta condición se ha.
La disolución gaseosa en líquidos es regida por una ley conocida como la Ley de Henry. Ley de Henry En el buceo la ley de Henry junto a otros principios de física como la ley de Haldane son la base para la elaboración de las tablas de buceo ya que permiten calcular la absorción de gases inertes por los distintos tejidos del cuerpo. Esta ley se resume en la siguiente ecuación.
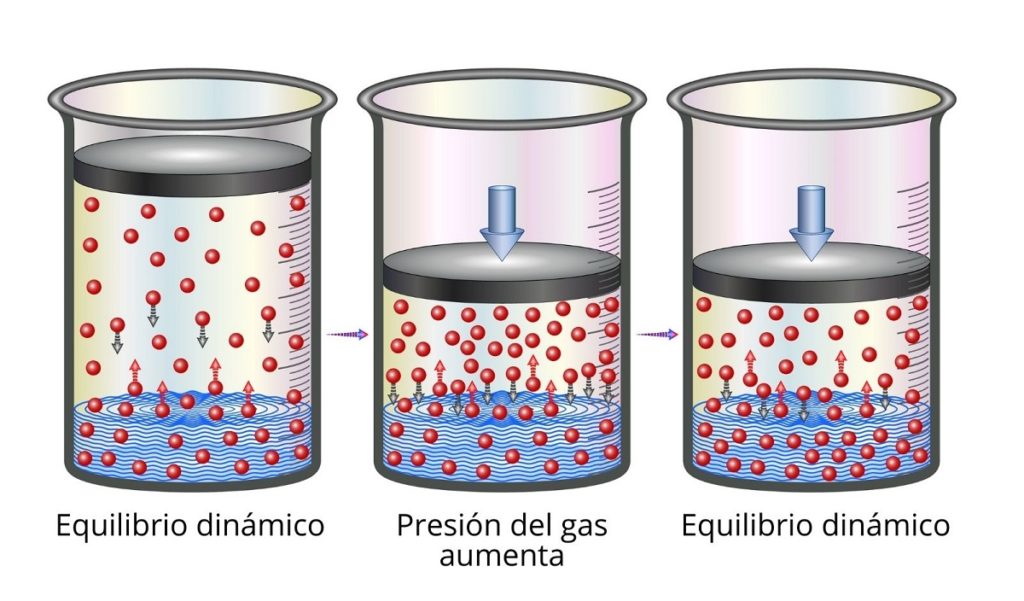
P kH c. Un ejemplo de la aplicación de esta ley está dado por las precauciones que deben tomarse al volver a un buzo a la superficie. La Ley de Henry.
LEY DE HENRY. Fue formulado por el químico inglés William Henry quien estudió el tema a principios del siglo XIXEn su publicación sobre la cantidad de.
En otras palabras la cantidad de gas disuelto es directamente proporcional a la presión. La ley establece que a temperatura constante la cantidad de gas disuelto en un volumen de un líquido especificado es directamente proporcional a la presión parcial del gas en equilibrio con el líquido. La Ley de Henry sostiene que la cantidad de gas disuelta en un líquido a una temperatura constante es directamente proporcional a la presión del gas sobre el líquido.
Por ejemplo en el proceso de intercambio de gas en la respiración la solubilidad del dióxido de carbono cuando están en contacto con el plasma del cuerpo es alrededor de 22 veces la del oxígeno. 3125 103 2 2.

Ley De Henry Y Ley De Raoult Biosep Liq Liq

Ley De Henry Es Util Para Gases Permanentes Es Decir Por Encima Del Punto Critico Por Ejemplo En El Caso De Una Disolucion De O2 En Agua El O2 No Ppt

Ejercicios De Ley De Henry Youtube
Ley De Henry Acuarios Plantados

Solubilidad De Gases Ley De Henry

Solubilidad De Gases Ley De Henry

Ley De Henry Y Ley De Raoult Biosep Liq Liq

Quimicas Ejemplos De La Ley De Raoult

Quimicas Ejemplos De La Ley De Dalton
Ley De Henry Explicacion Formula Ejemplos Excepciones

Ley De Henry Es Util Para Gases Permanentes Es Decir Por Encima Del Punto Critico Por Ejemplo En El Caso De Una Disolucion De O2 En Agua El O2 No Ppt

Solubilidad De Gases Ley De Henry

Ley De Henry Es Util Para Gases Permanentes Es Decir Por Encima Del Punto Critico Por Ejemplo En El Caso De Una Disolucion De O2 En Agua El O2 No Ppt

Ley De Henry Explicacion Formula Ejemplos Excepciones

Ley De Henry Disolucion Gas En Liquido Ejemplo 3 Youtube







Post a Comment for "Ley De Henry Ejemplos"